Jumlah atom 2 harus berbeda. Senyawa kovalen tidak larut dalam pelarut polar namun larut dalam pelarut organik.

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection
Atom logam setelah melepaskan elektron berubah menjadi ion positif.

. Senyawa kovalen tidak memiliki kemampuan ini karena mereka tidak mengandung ion. Senyawa polar terbentuk dari ikatan kimia dengan nama ikatan kovalen polar sedangkan senyawa nonpolar terbentuk dari ikatan kovalen nonpolar. Ikatan ion terbentuk antara atom yang melepaskan elektron logam dengan atom yang menangkap elektron bukan logam.
Senyawa dengan ikatan kovalen biasanya memiliki entalpi penguapan dan fusi yang lebih rendah. Atom N pada molekul amonia NH3 mempunyai. Hal tersebut terjadi karena senyawa kovalen polar dalam air akan terdissosiasi menjadi ion-ionnya.
Dari gambar struktur lewis di atas maka senyawa yang berikatan kovalen polar adalah senyawa NH 3 HF dan H 2 O sedangkan senyawa yang berikatan kovalen nonpolar adalah CH 4. Memiliki titik didih dan titik leleh yang relatif rendah. Senyawa ionik adalah senyawa yang atom-atomnya berikatan secara ionik.
Ada tiga jenis ikatan dalam molekulsenyawa yaitu ikatan ion ikatan kovalen polar dan kovalen non polar. Beberapa senyawa kovalen polar yang larut dalam air ada yang dapat menghantarkan arus listrik karena dapat terhidrolisis membentuk ion ion. Beberapa sifat senyawa kovalen yaitu meliputi.
HF asam florida. Lelehan wujud ini dapat menghantarkan listrik karena dalam bentuk lelehan ion-ionnya bergerak relatif bebas. Ikatan kovalen polar adalah ikatan yang pasangan elektron ikatannya cenderung tertarik ke salah satu atom yang berikatan.
Dapat menghantarkan arus listrik. Senyawa kovalen tidak dapat menghantarkan listrik. Senyawa ion juga lebih larut dalam air dibandingkan senyawa kovalen.
Suatu ikatan kovalen bersifat polar apabila distribusi elektron. HCl aq H aq Cl aq H 2 SO 4 aq 2 H aq SO 4 2 aq Beberapa senyawa kovalen polar tidak terdissosiasi sempurna dalam pelarut air sehingga memiliki kemampuan daya. Meski demikian senyawa kovalen dan ionik memiliki beberapa perbedaan dalam menghantarkan arus listrik.
Suatu ikatan kovalen disebut nonpolar apabila PEI tertarik sama kuat ke. Jenis Ikatan Molekul. Suatu ikatan kovalen disebut polar apabila PEI tertarik lebih kuat kesalah satu atom.
Senyawa ionik terbentuk oleh transfer elektron yang bermuatan. Kovalen polar dan non polar dimasukkan dalam kelompok kovalen. Sifat-sifat senyawa kovalen adalah.
Pada suhu kamar berbentuk gas ada juga yang berwujud cair dan padat. Akan tetapi cara menggambarkan struktur lewis satu per satu terasa kurang efisien jika dalam soal terdapat lebih dari 5 jenis senyawa. Jadi senyawa kovalen tidak bisa menghantarkan listrik.
Kepolaran suatu senyawa dapat ditentukan dari perbedaan keelektronegatifan atom-atom yang membentuk suatu senyawa kovalen. Senyawa kovalen berwujud lunak dan tidak mudah rapuh. Contoh Larutan Elektrolit Senyawa Kovalen Polar.
Ciri-ciri ikatan kovalen polar yaitu. KEPOLARAN SENYAWA KOVALEN Polaritas adalah pemisahan muatan yang terjadi pada suatu ikatan atau molekul disebabkan penyebaran elektron ikatan yang tidak merata pada kedua atom berikatan. Hal ini karena air melarutkan zat polar yang merupakan konsistensi senyawa ionik sedangkan senyawa kovalen non-polar.
Berbeda dengan senyawa ionik senyawa kovalen tidak mempunyai elektron yang bebas bergerak. Deya Hetri Safira 16030654022 Annisa Aura Lelyani 16030654028 Febrina Hanif Addaafi 16030654041 Karennina Putri A. 16030654057 UNIVERSITAS NEGERI SURABAYA JURUSAN IPA 20162017 FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM 1 Bab I Pendahuluan 11 Latar.
Sekarang kami akan bahas sedikit tentang apa perbedaan antara Senyawa dengan ikatan kovalen polar dan non polar. Ikatan Kovalen- Ikatan ion adalah ikatan yang terjadi akibat perpindahan elektron dari satu atom ke atom lain James E. Ikatan ionik adalah ikatan yang dihasilkan dari perpindahan elektron dari satu atom ke atom lain.
Senyawa kovalen polar biasanya terjadi antara atom-atom unsur yang beda keelektronegatifannya besar mempunyai bentuk molekul asimetris dan mempunyai momen dipol tidak sama dengan nol 0. Kepolaran ikatan terjadi karena adanya perbedaan keelektronegatifan. Sedangkan senyawa ion banyak yang tidak membakar.
Untuk memahami perbedaan wujud senyawa ionik dan kovalen polar ini berikut penjelasannya. Satu atom memberikan satu atau lebih dari elektron. Jika dua atom nonlogam sejenis diatomik membentuk suatu senyawa kovalen misalkan H2 N2 Br2 dan I2 maka ikatan kovalen yang terbentuk memiliki keelektronegatifan yang sama atau tidak.
Ikatan ion terbentuk akibat gaya elektrostatik antara ion-ion berlawanan muatan yang terjadi karena adanya serah terima elektron dari satu atom ke atom. Ikatan kovalen koordinasi hanya dapat terjadi jika salah satu atom mempunyai pasangan elektron bebas PEB. Senyawa kovalen koordinasi adalah ikatan kovalen di mana pasangan elektron yang dipakai bersama hanya disumbangkan oleh satu atom sedangkan atom yang satu lagi tidak menyumbangkan elektron.
Banyak sekali senyawa kovalen yang mudah terbakar terutama yang mengandung hidrogen dan karbon. Senyawa kovalen polar hanya dapat menghantarkan listrik dalam larutan dan senyawa kovalen nonpolar tidak dapat menghantarkan listrik. Padatan wujud ini tidak dapat menghantarkan listrik karena dalam bentuk padatan tidak ada ion yang bergerak secara bebas.
Karena sifat inilah senyawa polar mampu menghantarkan arus listrik. HF HCl dan HBr. LAPORAN RESMI KIMIA SENYAWA ION DAN SENYAWA KOVALEN Oleh Kelompok 10.
Senyawa kovalen memiliki titik didih dan titik leleh yang rendah. Ikatan kovalen polar adalah ikatan kovalen dimana pasangan elektron yang dipakai bersama cenderung tertarik ke salah satu atom yang berikatan.

Perbedaan Senyawa Ion Senyawa Kovalen Dan Logam Utakatikotak Com
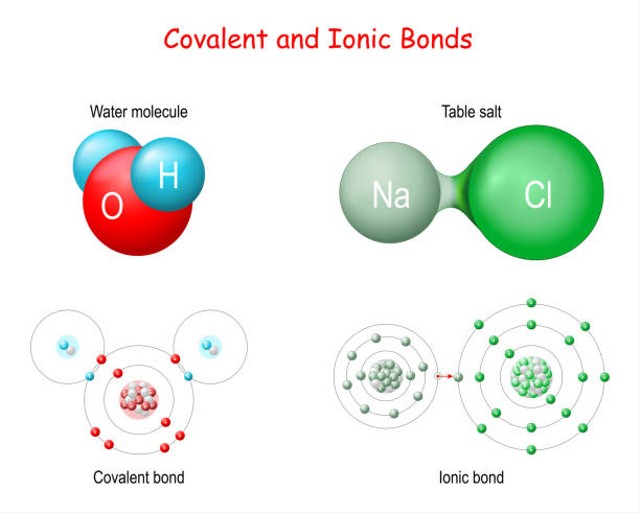
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com
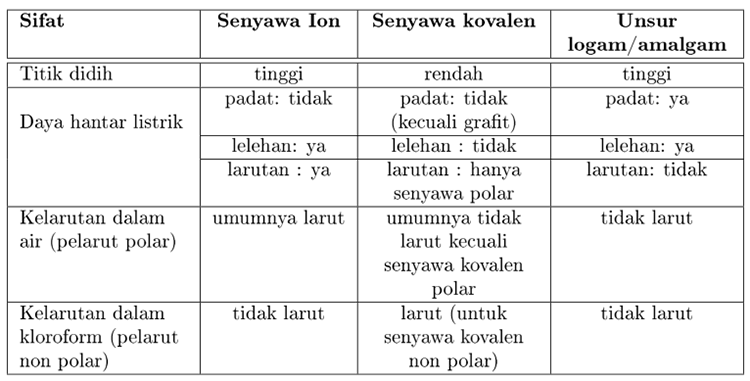
Modul Rumus Soal Sifat Fisis Senyawa Wardaya College
![]()
Perbedaan Sifat Senyawa Ion Dan Senyawa Kovalen Po

Ciri Ciri Dari Senyawa Ion Dan Senyawa Kovalen Brainly Co Id

Contoh Senyawa Ion Beserta Namanya

Bandingkan Sifat Senyawa Ionik Dan Senyawa Kovalen

1 Senyawa Kovalen Polar Dan Non Polar Ppt Download
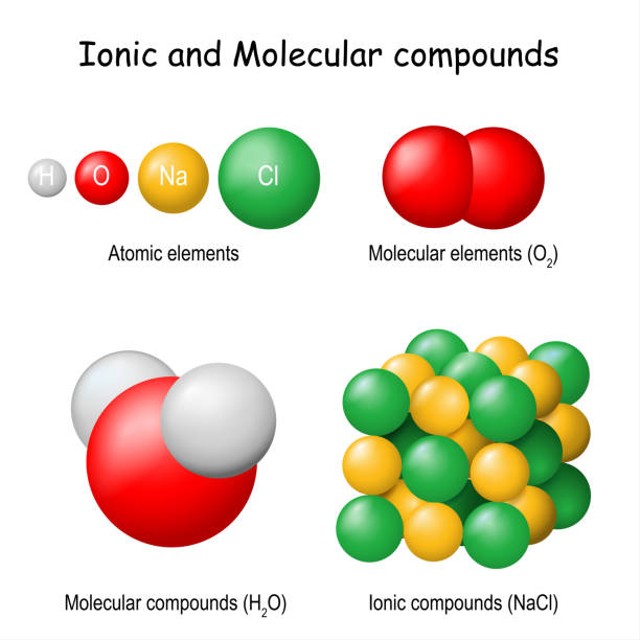
Perbedaan Senyawa Ionik Dan Senyawa Kovalen Polar Kumparan Com
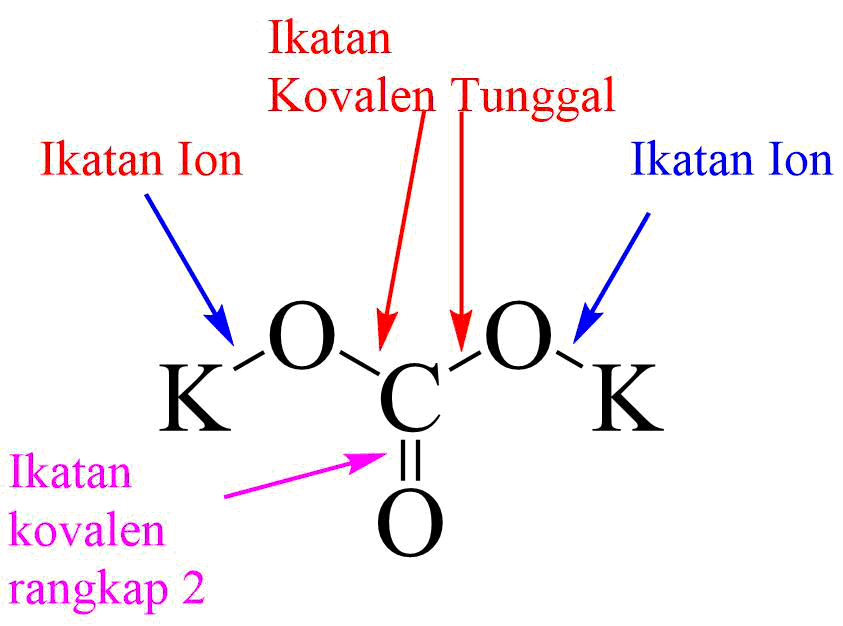
19 Contoh Senyawa Yang Mempunyai Ikatan Ion Dan Kovalen Sekaligus Materi Kimia

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Pengertian Senyawa Kovalen Polar Dan Nonpolar Serta Perbedaannya

Ikatan Kovalen Polar Dan Nonpolar Penjelasan Perbedaan Dan Contoh

Senyawa Kovalen Polar Pengertian Contoh Dan Ciri Cirinya

Sebutkan Sifat Atau Ciri Senyawa Kovalen Dan Ion Brainly Co Id

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Poster Ikatan Kimia Ikatan Kimia Kimia Panduan Belajar

Daya Hantar Listrik Senyawa Ion Kovalen Polar Kovalen Nonpolar Part 8 Otosection

Ciri Ciri Ikatan Ion Ikatan Kovalen Polar Dan Nonpolar Brainly Co Id
